Forschungsschwerpunkte
Forschungsschwerpunkte
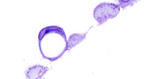
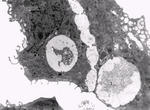
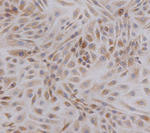
Die zentrale Kompetenz unserer Arbeitsgruppe liegt in der Etablierung von realitätsnahen in vitro Modellen der Angiogenese und Vaskulogenese. Vaskulogenese nennt man die Determination und Differenzierung endothelialer Progenitorzellen aus dem Mesoderm und ihre de novo Organisation zu einem primitiven Gefäßnetz. Im Anschluss an die Vaskulogenese kommt es zur Angiogenese, der Entwicklung neuer Kapillaren aus bereits existierenden Blutgefäßen durch Migration, Proliferation und dreidimensionale Organisation der vaskulären Endothelzellen.
Angiogenese und ihre Hemmung, die Antiangiogenese, sind im Fokus modernster Medizin. Vor allem die Hemmung der pathologischen Neoangiogenese (z.B. in Tumoren) stellt derzeit in Kombination mit konservativen Methoden, wie der Chemo- und Strahlentherapie, die einzige effektive Tumortherapie dar. Daher werden im Bereich der Angiogenese-Forschung zahlreiche Tierversuche durchgeführt. Unsere in vitro Modelle bieten für die Identifizierung und Untersuchung pro- und antiangiogener Substanzen eine Alternative zum Tierversuch. Sie basieren auf der Isolierung, Charakterisierung und Kultivierung mikrovaskulärer Endothelzellen verschiedener Spezies (Mensch, Rind, Maus, Schwein, Hund) und mehrerer Organe (Haut, Corpus luteum, Herz, Ovar, Milz etc.). Diese Kulturen zeigen alle Phasen der Angiogenese einschließlich der Bildung tubulärer und lumenisierter Strukturen, die in den verschiedenen Modellen zwei- oder dreidimensional ausgeprägt sind. Dabei hat sich gezeigt, dass in den Kulturen auch endotheliale Stamm- und Progenitorzellen an der Bildung der gefäßähnlichen Strukturen beteiligt sind.
Durch eine bereits intern validierte Methode zur Quantifizierung der in vitro Angiogenese kann die Wirkung pro- bzw. antiangiogener Substanzen auf zellulärer Ebene untersucht werden. Für den laborübergreifenden Einsatz unter Routinebedingungen wird die Standardisierung und externe Validierung dieser Methode angestrebt.
Forschungskompetenzen
Angiogenese
Isolierung mikrovaskulärer Endothelzellen und Etablierung dreidimensionaler in vitro Modelle der Blutgefäßbildung
Spezies: Rind, Schwein, Hund, Maus, Pferd, Mensch
Organe: Ovar, Corpus luteum, Herz, Hoden, Gehirn, Milz, Vorhaut
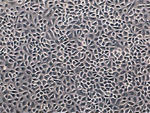
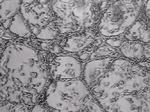
Vaskulogenese
Isolierung primitiver Endothelzellen aus dem porzinen Dottersack
In vitro-Differenzierung endothelialer Stammzellen des Rhesusaffen zu funktionellen Endothelzellen (Kooperationsprojekt)
Charakterisierung von Stamm- und Progenitorzellen im adulten Rind
Pathologische Gefäßbildung
Isolierung, Kultivierung und Charakterisierung transformierter Endothelzellen
Etablierung eines in vitro Modells des malignen Hämangioendothelioms aus dem murinen Myokard und der caninen Milz
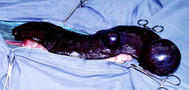

Zelluläre Regulation der Gefäßbildung
Entwicklung, Lumenbildung, Remodelling und Regression (Anti-Angiogenese) von Blutgefäßen
Quantifizierung der Angiogenese bzw. Anti-Angiogenese
Vaskuläre Mimikry
Molekulare Regulation der Gefäßbildung
Vascular Endothelial Growth Factor (VEGF)
VEGF-Rezeptoren
Angiopoietine
Kallikrein-Kinin-System
Stammzellantigene
Gentechnische Manipulation der Gefäßbildung
Transfektion von Endothelzellen in vitro
Charakterisierung von Plasmidkonstrukten
Spezifität und Expressionsstärke unterschiedlicher Promotoren